鉻(Ⅵ)的方波伏安行為和測定
| 論文類型 | 基礎研究 | 發表日期 | 2004-06-01 |
| 來源 | 《工業用水與廢水》2004年第3期 | ||
| 作者 | 許琦,嚴金龍,楊春生 | ||
| 關鍵詞 | 方波伏安法 鉻(Ⅵ) 廢水測定 環境分析 | ||
| 摘要 | 在0.1 mol/L的氨水緩沖溶液(pH=10.0)中,鉻(Ⅵ)離子于-1.45V(vs S.C.E)出現一靈敏的方波伏安峰。峰電流Ip與Cr(Ⅵ)的質量濃度在0.1~2.0× 103m/L范圍內呈現良好的線性關系,其相關系數為0.9886,檢出限為0.05mg/L Cr(Ⅵ),方法的標準偏差為2.8%。該法應用于實際樣品電鍍鉻液及其廢液中鉻(Ⅵ)含量的測定,結果表明:與標準方法二苯碳酰二肼分光光度法比較,本法不需要加入特定的試劑而直接水樣測定,簡單快速。 | ||
許琦,嚴金龍,楊春生
(鹽城工學院 化學工程系,江蘇 鹽城 224003)
摘要:在0.1 mol/L的氨水緩沖溶液(pH=10.0)中,鉻(Ⅵ)離子于-1.45V(vs S.C.E)出現一靈敏的方波伏安峰。峰電流Ip與Cr(Ⅵ)的質量濃度在0.1~2.0× 103m/L范圍內呈現良好的線性關系,其相關系數為0.9886,檢出限為0.05mg/L Cr(Ⅵ),方法的標準偏差為2.8%。該法應用于實際樣品電鍍鉻液及其廢液中鉻(Ⅵ)含量的測定,結果表明:與標準方法二苯碳酰二肼分光光度法比較,本法不需要加入特定的試劑而直接水樣測定,簡單快速。
關鍵詞:方波伏安法;鉻(Ⅵ);廢水測定;環境分析
中圖分類號:X830.2 文獻標識碼:B 文章編號:1009-2455(2004)03-0051-03
Square-Wave Voltampere Behavior of Cr(Ⅵ) Ion and Its Determination
Xu Qi,YAN Jin-long,YANG Chun-sheng
(Department of Chemical Engineering,Yancheng Institute of Technology,Yancheng 224003,China)
Abstract:Chromium (Ⅵ) ion showed a sensitive square-wave voltampere peak at -1.45 V(vs S.C.E) in the buffer solution of 0.1 mol/L ammonia liquor (pH=10.0).There appeared a good linear relationship between the peak current Ip and the mass concentration of Cr(Ⅵ) when it was within the range of 0.1~2.0×103mg/L,the correlation coefficient of which was 0.9886,the detection limit was 0.05 mg/L Cr(Ⅵ),and the standard deviation was 2.8%.The said method was used in determining the chrome (Ⅵ) contents in the sample of actual chrome plating solution and the waste liquor,the results of which showed that compared with spectrophotography with 1,5-Diphenylcarbohydrazide,which is a standard method,this method does not need the addition of specific reagent but directly determines the water sample,which is simple and quick.
Key words:square-wave voltampere method;chromium (Ⅵ);wastewater determination;environmental analysis
環境中的鉻主要以無機鉻和有機鉻兩種形態存在,其中無機鉻的含量遠比有機鉻大得多,而無機鉻中常見的形態為鉻(Ⅲ)和鉻(Ⅵ)。鉻及其化合物在工業中應用廣泛,能夠以各種形式進入環境。有關工廠的廢水、廢氣排放都對環境造成了較大的污染,是環境污染監測中的必測項目之一。因此,研究一種簡單、快速而準確測定鉻(Ⅵ)離子的方法就顯得非常的重要[1-3]。
到目前為止,已報道了許多測定環境中鉻(Ⅵ)的方法。主要有分光光度法、原子光譜分析法等[4-6],但有的試劑選擇性較差,用于某些復雜樣品分析時,常需借助適當的分離富集手段以消除干擾,有的儀器設備復雜。電化學分析法雖然有報道,但體系復雜,一般是采用極譜催化波或絡合吸附波,分析時通過選擇合適的氧化還原體系改變鉻的存在價態,結合特定的研究方法測定總量,采用差減法測定各單一價態鉻的含量[4]。而分光光度法是國內外的標準方法,利用在酸性介質中,六價鉻與二苯碳酰二肼(DPC)反應,生成紫紅色絡合物,于540nm波長處進行比色測定[1]。
本文研究了鉻(Ⅵ)在NH3-NH4C1(pH=10.0)介質條件下的電化學行為,并依此建立了方波伏安法快速分析環境中的鉻(Ⅵ),方法的線性范圍為0.1~2.0×103mg/L,檢出限為0.05mg/L,方法簡單、快速,應用于實際樣品電鍍鉻液及其廢液中鉻(Ⅵ)含量的測定,結果滿意。
1 實驗部分
1.1 主要儀器及試劑
CHI832電化學分析儀;三電極系統:汞膜電極為工作電極,鉑電極為輔助電極,甘汞電極為參比電極;SRD-1型磁力攪拌器。
鉻標準溶液:5.0g/L,準確稱取基準重鉻酸鉀1.25g于100mL燒杯中,少量蒸餾水溶解,轉移到250mL容量瓶中,并定容。其它濃度的溶液,由此溶液稀釋所得。
氨水緩沖溶液(pH=10.0):1 mol/L,將54gNH4Cl溶于水中,加人濃氨水350mL,稀釋 1.OL。
飽和Na2SO3溶液。
試劑皆為分析純,水為二次蒸餾水。
1.2 試驗方法
準確移取氨水緩沖溶液2.00mL于20mL比色管中,加入飽和Na2SO3溶液4.00mL和一定量的鉻標準溶液,定容后攪拌除氧10min。插入電極,控制起始電位為 -1.00 V,負向掃描 -1.6V,在電化學分析儀上記錄方波伏安峰,測其在 -1.45V(vs S.C.E,相對于飽和甘汞電極,下同)處的方波伏安電流峰高Ip。
2 結果與討論
2.1 鉻的方波伏安峰
在O.1 mol/L的氨水緩沖溶液中,Cr(Ⅵ)在汞膜電極上于 -1.45V(vs S.C.E)處出現一靈敏的方波伏安峰,伏安圖波形較好,且峰電流Ip與Cr(Ⅵ)的濃度在一定的范圍內呈線性關系,而氨水緩沖溶液底液無峰(見圖1)。
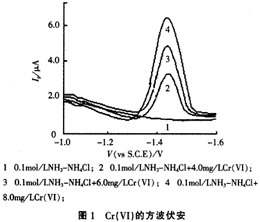
方波伏安技術用于物質的測定,具有靈敏度高、分辨率好、前波影響小等特點,圖1結果表明:將其用于Cr(Ⅵ)的定量分析,緩沖底液、溶解氧及其它雜質對Cr(Ⅵ)方波伏安峰均無干擾,峰型對稱,利于測定。
2.2 支持電解質的選擇
考察了Cr(Ⅵ)在不同濃度和pH值的NH3-NH4Cl緩沖溶液、硼砂緩沖溶液、KOH溶液、KCl、B-R緩沖溶液等多種緩沖體系中的伏安行為,發現僅在氨水緩沖體系中波形良好、靈敏度高。氨水溶液濃度≥5.0× 10-3mol/L時,伏安峰靈敏且穩定,本法選擇0.1 mol/L,氨水溶液作為測定介質。
2.3 電化學實驗條件的選擇
隨著方波頻率增大,金屬離子峰電流逐漸增大,峰電位負移,但半峰寬也增大,對測定不利,本法選擇頻率為35Hz。靜止時間在10s之后,波峰達到最大且穩定,本法選取靜止時間為10s,電位掃描速度為4mV/s。
起始電位在 -0.8~-1.1V之間時,峰電流基本不變化,本實驗選擇-1.0V作為測定的起始電位。
2.4 循環伏安圖
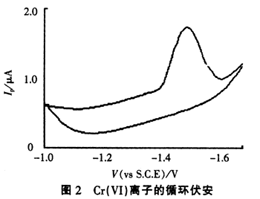
在0.1 mol/L的氨水緩沖溶液中,質量濃度為5.0mg/LCr(Ⅵ)離子的循環伏安圖示于圖2。循環伏安圖表明在陰極分支上有還原峰,陽極分支無氧化峰,說明Cr(Ⅵ)離子在汞膜電極上的電極反應過程為不可逆過程。
2.5 線性范圍和檢出限
在上述最佳條件下,峰電流Ip與Cr(VI)的質量濃度在0.1~2.0×103mg/L范圍內呈現良好的線性關系,其回歸方程為Ip(μA)=0.2870+0.6424C(mg/L),相關系數為0.9886,檢出限為ρ(Cr6+)=0.05mg/L。
2.6 共存離子的影響
pH=10.0的氨水緩沖溶液中,ρ(Cr6+)=5.0mg/L條件下,相對誤差≤±5%時,允許以下離子(倍數)共存:K+,Na+,Al3+,NH4+,Mg2+,Ca2+,NO3-, SO42-(5.0× 103), Mn2+(1000), Cu2+(500),Fe3+(350), Cr3+(210), Cd2+(175), Fe2+(142), Zn2+(50)不影響測定。
2.7 合成水樣分析
對質量濃度為5.0mg/L Cr(Ⅵ)的合成標準樣進行了6次平行測定,方法的相對標準偏差為2.8%,說明實驗所建立的方法具有很高的精密度,結果見表1。
表1 合成水樣分析結果
合成樣品
ρ(Cr6+)/(mg·L-1)
測定值
ρ(Cr6+)/(mg·L-1)
平均測定值
ρ(Cr6+)/(mg·L-1)
相對標準偏差/%
5.0
4.92
4.98
4.98
5.02
2.8 5.04 5.10 5.10
2.8 電鍍廢液和鍍鉻溶液中Cr(Ⅵ)分析
吸取適量樣品溶液并調節pH值近中性,經陽離子交換樹脂處理后,溶液于25 mL容量瓶中定容。準確移取適量溶液于電解池中,按實驗方法進行測定。并于二苯碳酰二肼標準方法測定結果進行對照,表明無顯著性差異,結果見表2。
表2 樣品分析結果
樣品
ρ(Cr6+)/(mg·L-1)
回收率/%
本法
標準法
加入量
本法總量
電鍍廢液1
1.08
1.12
1.00
2.07
99.0
電鍍廢液2
2.84
2.90
2.00
4.85
100.5
渡鉻溶液
198.6
200.4
100.0
300.2
101.6
*表中所有的分析結果皆為6次分析結果的平均值。
參考文獻:
[1] 蔡宏道.環境污染與衛生監測[M].北京:人民衛生出版社,1981.
[2] 康新平,劉洪海,陳堅.液體樣品中鉻的價態和微量分析的研究進展[J].理化檢驗-化學分冊,1999,35(3):139-142.
[3] 柴之芳,祝漢民.微量元素化學概論[M].北京:原子能出版社,1994.
[4] 魏顯有,王秀敏,劉云惠,等.鉻(Ⅵ)-硫脲體系的極譜吸附波及其應用于土壤中總鉻和有效鉻(Ⅵ)的測定[J].分析化學,1996, 24(10): 1170-1174.
[5] 馮素玲,唐安娜,樊靜.熒光分析法測定痕量鉻Ⅵ[J].分析化學,2001,29(5):558-560.
[6] 嚴金龍.用甲殼素富集光度法測定廢水中的微量鉻離子[J].材料保護,2001,34(11):39-40.
作者簡介:許琦(1965-),男,江蘇鹽城人,副教授,博士,現 主要從事化工機械及環保有關的教學、科研工作。
論文搜索
發表時間 至
月熱點論文
論文投稿
很多時候您的文章總是無緣變成鉛字。研究做到關鍵時,試驗有了起色時,是不是想和同行探討一下,工作中有了心得,您是不是很想與人分享,那么不要只是默默工作了,寫下來吧!投稿時,請以附件形式發至 paper@h2o-china.com ,請注明論文投稿。一旦采用,我們會為您增加100枚金幣。








